ж–Үз« |2020е№ҙ10еҲҶ+зәҜз”ҹдҝЎж–Үз« еёҰдҪ йўҶз•ҘNatureеӯҗеҲҠд№Ӣй©ұеҠЁзӘҒеҸҳж–Үз« еҘ—и·Ҝ
е°Ҹдјҷдјҙ们еӨ§е®¶еҘҪпјҢд»ҠеӨ©еёҰз»ҷеӨ§е®¶дёҖзҜҮй«ҳеӨ§дёҠзҡ„зәҜз”ҹдҝЎж–Үз« пјҢ2020е№ҙ2жңҲеҸ‘иЎЁеңЁNatureеӯҗеҲҠдёҠпјҢеҪұе“Қеӣ еӯҗ12.121пјҢйўҳзӣ®дёәвҖңPathway and network analysis of more than 2500 whole cancer genomesвҖқгҖӮжҳҜдёҖзҜҮеҹәдәҺеҺҹеҸ‘иӮҝзҳӨзҡ„WGSж•°жҚ®ж•ҙеҗҲеҲҶжһҗвҖ”вҖ”PCAWGи®ЎеҲ’зҡ„ж–Үз« пјҢеӨ§е®¶д№ҹдёҚеҝ…дёҠжқҘе°ұеҜ№иҝҷз§Қй«ҳз«Ҝзҡ„ж•ҙеҗҲеҲҶжһҗжңӣиҖҢз”ҹз•ҸпјҢеҚідҫҝжҳҜ10еҲҶ+зҡ„з”ҹдҝЎж–Үз« еҗҢж ·жңүеҘ—и·ҜпјҢиҖҢдё”зұ»дјјзҡ„ж–Үз« еңЁиҝҷдёӘеӣўйҳҹзҡ„жҲҗжһңз§Қд№ҹжҳҜдёҖеҸ‘дёҖеӨ§жҠҠгҖӮжҺҢжҸЎе…¶дёӯдёҖзӮ№зІҫй«“е°ұеӨҹжҲ‘们иҝҷдәӣз§‘з ”з•Ңзҡ„е°ҸжңӢпјҲиҸңпјүеҸӢпјҲйёЎпјүеЎ«йҘұиӮҡеӯҗдәҶгҖӮ
ж–Үз« еӣҫзүҮ
ж—©еңЁ2013е№ҙпјҢеӨ§е®¶и¶…зә§зҶҹжӮүзҡ„TCGAзҡ„Pan-Cancerж•°жҚ®еә“е°ұзі»з»ҹжҖ§зҡ„规еҲ’еҘҪдәҶгҖӮеӣ дёәTCGAи®ЎеҲ’ж¶үеҸҠеҲ°ж•°жҚ®зұ»еһӢжҜ”иҫғеӨҡпјҢд»…д»…жҳҜDNAеұӮйқўе°ұжңүWGS,WES,SNP6.0иҠҜзүҮзҡ„ж•°жҚ®пјҢеңЁж”¶еҪ•зҡ„дёҖдёҮеӨҡж ·жң¬з§ҚжңүWGSж•°жҚ®зҡ„жңүдёӨеҚғеӨҡдёӘпјҢPCAWGи®ЎеҲ’е°ұгҖӮжҳҜж•ҙеҗҲиҝҷе…¶дёӯжүҖжңүзҡ„WGSж•°жҚ®з»“жһңгҖӮдёӢйқўжҲ‘们е°ұжқҘеҲҶжһҗдёҖдёӢиҝҷзҜҮ10еҲҶ+зәҜз”ҹдҝЎж–Үз« зҡ„з ”з©¶еҘ—и·Ҝеҗ§пјҢеёҰеӨ§е®¶еҸ‘зҺ°еҚідҫҝжҳҜ10еҲҶ+з”ҹдҝЎж–Үз« д№ҹйҖғдёҚиҝҮй…ёиҸңж Ўй•ҝжҖ»з»“зҡ„вҖңжҢ‘гҖҒеңҲгҖҒиҒ”гҖҒйқ вҖқеӣӣеӯ—иҜҖпјҒ
ж–Үз« еӣҫзүҮ
з ”з©¶иғҢжҷҜ
жңүдёҖдәӣи§ӮзӮ№и®ӨдёәзҷҢз—ҮеҸ‘з”ҹзҡ„ж №жң¬еҺҹеӣ жҳҜеҹәеӣ зӘҒеҸҳгҖӮд»ҺиЎЁзҺ°еҪўејҸдёҠжқҘи®ІжҳҜиӮҝзҳӨз»ҶиғһдёҚеҸҜжҺ§еҲ¶зҡ„еўһй•ҝпјҢдё»иҰҒжҳҜиӮҝзҳӨй©ұеҠЁеҹәеӣ зӘҒеҸҳеҜјиҮҙпјҢиҝҷдәӣеҹәеӣ еҸ‘з”ҹзӘҒеҸҳеҗҺпјҢзү№еҲ«жҳҜжҹҗдәӣеҹәеӣ еҸ‘з”ҹйҮҚеӨ§зӘҒеҸҳпјҢиӮҝзҳӨзҡ„еҸ‘з”ҹеҸҜиғҪе°ұжҲҗдёәдәҶдёҖз§Қеҝ…然гҖӮз»қеӨ§еӨҡж•°е·ІзҹҘзҡ„й©ұеҠЁзӘҒеҸҳеҪұе“ҚиӣӢзҷҪиҙЁзј–з ҒеҢәеҹҹгҖӮ
дҪҶеңЁи®ёеӨҡзҷҢз—ҮдёӯпјҢзӣёеҪ“жҜ”дҫӢзҡ„жӮЈиҖ…еңЁиӣӢзҷҪиҙЁзј–з ҒеҢәжІЎжңүе·ІзҹҘзҡ„й©ұеҠЁзӘҒеҸҳпјҢиҝҷиЎЁжҳҺеҸҰжңүдёҖйғЁеҲҶй©ұеҠЁзӘҒеҸҳд»ҚжңӘиў«еҸ‘зҺ°гҖӮеӣ жӯӨпјҢжҺўзҙўжӣҙеӨҡиӣӢзҷҪиҙЁзј–з Ғеҹәеӣ зҡ„зҷҢз—Үй©ұеҠЁзӘҒеҸҳжҲҗдәҶеҪ“д»ЈиӮҝзҳӨиҜҠз–—зҡ„зЎ¬жҖ§йңҖжұӮгҖӮзӣ®еүҚиӣӢзҷҪиҙЁзј–з Ғеҹәеӣ зҡ„зҷҢз—Үй©ұеҠЁзӘҒеҸҳе·Із»Ҹз ”з©¶зҡ„еҫҲе……еҲҶдәҶгҖӮ然иҖҢпјҢеҜ№йқһзј–з ҒзҷҢз—Үй©ұеҠЁзӘҒеҸҳзҡ„з ”з©¶е°ҡеҫ…ејҖеҸ‘пјҢеҸӘжңүе°‘ж•°еӨҚеҸ‘жҖ§йқһзј–з ҒзӘҒеҸҳпјҢжңҖжҳҫи‘—зҡ„жҳҜTERTеҗҜеҠЁеӯҗзӘҒеҸҳгҖӮ
PCAWGпјҢжҳҜе…Ёеҹәеӣ з»„жіӣзҷҢеҲҶжһҗпјҲPan-Cancer Analysis of Whole Genomesпјүзҡ„з®Җз§°гҖӮ
дёҺд»ҘеүҚдё»иҰҒйӣҶдёӯдәҺзҷҢз—Үеҹәеӣ з»„зҡ„иӣӢзҷҪзј–з ҒеҢәеҹҹзҡ„з ”з©¶дёҚеҗҢпјҢPCAWGиҒ”зӣҹжҖ»е…ұй’ҲеҜ№38дёӘзҷҢз§ҚпјҢз»јеҗҲеҲҶжһҗдәҶж•ҙдёӘеҹәеӣ з»„пјҢжҳҜиҝ„д»ҠдёәжӯўжңҖе…Ёйқўзҡ„зҷҢз—Үеҹәеӣ з»„иҚҹиҗғеҲҶжһҗгҖӮиҝҷйЎ№з ”з©¶жңү6зҜҮNatureеҸҠеҚҒдҪҷзҜҮNatureеӯҗеҲҠж”Ҝж’‘пјҢеҲҶеҲ«еҜ№PCAWGж•°жҚ®йӣҶзҡ„е№ҝеәҰе’Ңж·ұеәҰиҝӣиЎҢдәҶиҜҰз»Ҷзҡ„жҺўи®ЁгҖӮ2019е№ҙ10жңҲпјҢеҸ‘иЎЁдәҺгҖҠNatureгҖӢдёҠзҡ„ж–Үз« гҖҠPan-cancer whole-genome analyses of metastatic solid tumoursгҖӢпјҢжҸҸиҝ°дәҶзӣ®еүҚе·ІзҹҘзҡ„жңҖеӨ§зҡ„иҪ¬з§»жҖ§е®һдҪ“зҳӨеҹәеӣ з»„зҡ„жіӣзҷҢз§Қз ”з©¶гҖӮеҲҶжһҗдәҶ2520еҜ№иӮҝзҳӨе’ҢжӯЈеёёз»„з»Үзҡ„е…Ёеҹәеӣ з»„жөӢеәҸж•°жҚ®пјҢе№іеқҮжөӢеәҸж·ұеәҰеҲҶеҲ«дёә106Xе’Ң38XпјҢе…ұйүҙе®ҡеҮә7000дёҮдёӘдҪ“з»ҶиғһзӘҒеҸҳгҖӮ
жҚ®жҠҘйҒ“жүҖи®әиҝ°пјҢжҜҸдёӘзҷҢз—Үеҹәеӣ з»„еқҮжҗәеёҰ4жҲ–5дёӘй©ұеҠЁзӘҒеҸҳпјҢиҝҷдёәиӮҝзҳӨз»ҶиғһжҸҗдҫӣдәҶйҖүжӢ©жҖ§дјҳеҠҝгҖӮеңЁжүҖз ”з©¶зҡ„38зұ»иӮҝзҳӨдёӯпјҢд»…5%жІЎжңүеҸ‘зҺ°й©ұеҠЁзӘҒеҸҳгҖӮзӣёжҜ”д№ӢдёӢпјҢи®ёеӨҡзҷҢз§ҚиЎЁзҺ°еҮәеӨҚжқӮзҡ„жҹ“иүІдҪ“йҮҚжҺ’гҖҒзўҺиЈӮзӯүзү№еҫҒпјҢд»ҺиҖҢеҜјиҮҙеҹәеӣ з»„еҸ‘з”ҹйҮҚеӨ§зҡ„з»“жһ„еҸҳеҢ–гҖӮ
з ”з©¶жҲҗжһңеҢ…жӢ¬жҸӯзӨәдәҶж–°зҡ„йқһзј–з Ғй©ұеҠЁеӣ еӯҗпјҢеҰӮжҠ‘зҷҢеҹәеӣ TP53йқһзј–з ҒеҢәдёӯеҸ‘з”ҹзҡ„еӨҚеҸ‘зӘҒеҸҳпјӣз«ҜзІ’й…¶еҹәеӣ TERTзҡ„йқһзј–з ҒеҢәдёӯзӣёеҜ№йў‘з№ҒеҸ‘з”ҹзҡ„зӘҒеҸҳеҜјиҮҙз«ҜзІ’й…¶зҡ„иҝҮеәҰиЎЁиҫҫпјӣе®Ңе–„е·ІзҹҘзҡ„зӘҒеҸҳж Үзӯҫ并еҸ‘зҺ°ж–°зҡ„зӘҒеҸҳж ҮзӯҫзӯүзӯүгҖӮжңүе…ҙи¶Јзҡ„е°ҸдјҷдјҙеҸҜд»ҘиҮӘиЎҢеӯҰд№ пјҢж–Үжң«дјҡжҸҗдҫӣз»ҷеӨ§е®¶иҝҷйЎ№з ”з©¶зӣёе…ізҡ„жүҖжңүж–Үз« пјҢжҳҜжүҖжңүе“Ұ~(в—Ҹ'"/>
ж–Үз« еӣҫзүҮ
в–І Fig.1
гҖҗ ж–Үз« |2020е№ҙ10еҲҶ+зәҜз”ҹдҝЎж–Үз« еёҰдҪ йўҶз•ҘNatureеӯҗеҲҠд№Ӣй©ұеҠЁзӘҒеҸҳж–Үз« еҘ—и·ҜгҖ‘вҖңеңҲвҖқгҖҒвҖңиҒ”вҖқвҖ”вҖ”дәӨдә’дҪңз”ЁеҸҠзӣёе…іжҖ§еҲҶжһҗ
1.жҪңеңЁй©ұеҠЁзӘҒеҸҳзҡ„йҖҡи·Ҝе’ҢзҪ‘з»ңеҲҶжһҗ
жҺҘдёӢжқҘ,дҪңиҖ…е°ұеҜ№жҪңеңЁзҡ„й©ұеҠЁзӘҒеҸҳиҝӣиЎҢйҖҡи·Ҝе’ҢзҪ‘з»ңеҲҶжһҗгҖӮ他们еҗҢж—¶дҪҝз”ЁдәҶдёӨз§ҚйҖҡи·Ҝз®—жі•:ActivePathwaysе’ҢдёҖз§Қи¶…еҮ дҪ•еҲҶжһҗз®—жі•вҖ”вҖ”Vazquezпјӣд»ҘеҸҠдә”з§ҚзҪ‘з»ңж–№жі•:CanIsoNetгҖҒHierarchical HotNetгҖҒиҜұеҜјеӯҗзҪ‘з»ңеҲҶжһҗгҖҒNBDI22е’ҢSSA-ME23гҖӮеҲ©з”Ёд»ҘдёҠйҖ”еҫ„е’ҢзҪ‘з»ңж•°жҚ®еә“пјҢдҪңиҖ…еҜ№GS-CгҖҒGS-Nе’ҢGS-CNеҹәеӣ иҜ„еҲҶиҝҗиЎҢжҜҸз§Қж–№жі•пјҢзЎ®е®ҡдәҶдёүдёӘзӣёеә”зҡ„еҹәеӣ еҲ—иЎЁгҖӮжҜҸз§Қж–№жі•еҜ№е…¶з»“жһңеңЁжҜҸдёӘж•°жҚ®йӣҶдёҠзҡ„з»ҹи®Ўжҳҫи‘—жҖ§иҝӣиЎҢиҜ„дј°гҖӮ
дҪңиҖ…йҖҡиҝҮзҪ‘з»ңдә’дҪңеҲҶжһҗи§ӮеҜҹеҲ°жҳҫи‘—зӘҒеҸҳзҡ„зј–з Ғе’Ң/жҲ–йқһзј–з Ғе…ғзҙ д№Ӣй—ҙеӯҳеңЁеӨ§йҮҸдәӨдә’пјҢиҝҷиЎЁжҳҺйҖҡи·Ҝе’ҢзҪ‘з»ңж–№жі•еҸҜиғҪжңүеҠ©дәҺдјҳе…ҲеӨ„зҗҶеҚ•дёҖе…ғзҙ еҲҶжһҗдёӯдёҚжҳҫи‘—зҡ„зҪ•и§Ғй©ұеҠЁдәӢ件гҖӮиҝҷд№ҹжҳҜиҝҷзҜҮз ”з©¶ж–ҮзҢ®зҡ„ж„Ҹд№үжүҖеңЁгҖӮ
еңЁе…·дҪ“зҡ„йҖҡи·Ҝе’Ңй©ұеҠЁеҲҶжһҗпјҢд»ҘзЎ®е®ҡй©ұеҠЁеҹәеӣ еңЁй•ҝе°ҫзҡ„й©ұеҠЁpеҖјзј–з Ғе’Ңйқһзј–з ҒзӘҒеҸҳдёӯпјҢд»…дҪҝз”Ёзј–з ҒзӘҒеҸҳеҸҜд»ҘиҜҶеҲ«еҮә87дёӘеёҰжңүзј–з ҒеҸҳејӮзҡ„йҖҡи·Ҝзүөиҝһй©ұеҠЁеҹәеӣ (PID-Cеҹәеӣ )пјҢе…¶дёӯеҢ…жӢ¬68дёӘд»ҘеүҚиў«COSMIC зҷҢз—Үеҹәеӣ жҷ®жҹҘ(CGC)ж•°жҚ®еә“зј–зӣ®зҡ„зҷҢз—Үеҹәеӣ гҖӮ并且其дёӯзҡ„31дёӘеҹәеӣ еңЁPCAWGеҲҶжһҗдёӯж— з»ҹи®ЎеӯҰж„Ҹд№үгҖӮиҜҙжҳҺд»ҘдёҠзҪ‘з»ңеҲҶжһҗеҸҜд»ҘзӯӣйҖүеҲ°е…·жңүзҪ•и§ҒзӘҒеҸҳзҡ„еҹәеӣ пјҢеҚійӮЈдәӣеңЁвҖңй•ҝе°ҫвҖқеҲҶеёғзҡ„пјҢеҸҜиғҪжҳҜй©ұеҠЁеҹәеӣ гҖӮдҪңиҖ…иҝҳеҸ‘зҺ°ж №жҚ®CGCж•°жҚ®еә“еҜ№жҜ”пјҢиҝҷ31дёӘFDR > 0.1зҡ„еҹәеӣ дёӯжңү13дёӘжҳҜе·ІзҹҘзҡ„й©ұеҠЁеӣ зҙ гҖӮдёҺйқһPID-Cеҹәеӣ зӣёжҜ”пјҢPID-Cеҹәеӣ зҡ„зј–з Ғеҹәеӣ еҫ—еҲҶжҳҺжҳҫиҫғй«ҳгҖӮ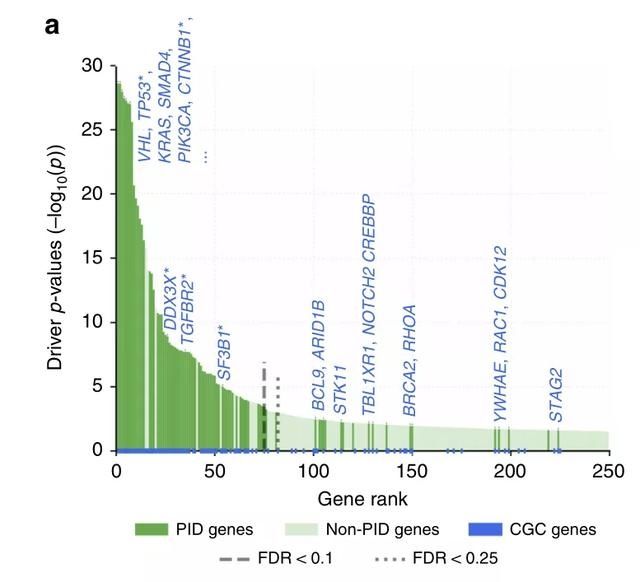
ж–Үз« еӣҫзүҮ
в–І Fig.2a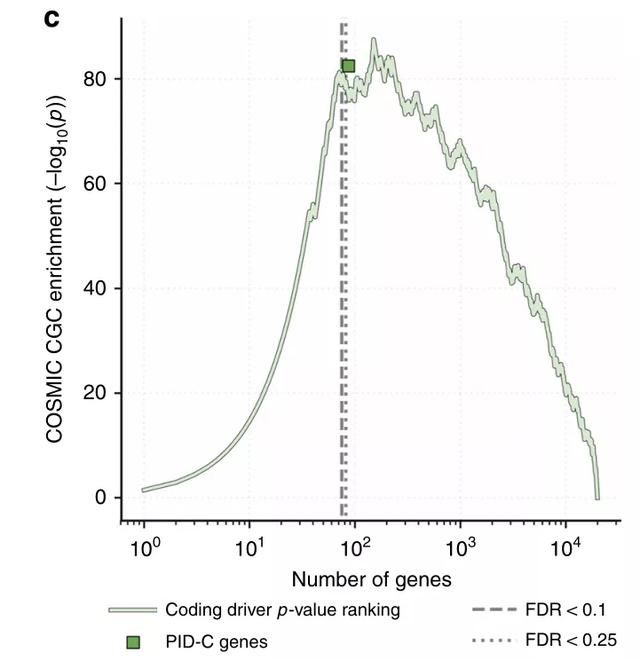
ж–Үз« еӣҫзүҮ
в–І Fig.2c
д»…дҪҝз”Ёйқһзј–з ҒзӘҒеҸҳпјҢдҪңиҖ…зЎ®е®ҡдәҶ62дёӘеҹәеӣ пјҢеҸ‘зҺ°зј–з ҒзӘҒеҸҳдёӯиҫғејәзҡ„дҝЎеҸ·еңЁзј–з Ғе’Ңйқһзј–з ҒзӘҒеҸҳдёӯеҚ дё»еҜјең°дҪҚгҖӮеӣ дёәйқһзј–з ҒзӘҒеҸҳжЈҖжөӢзҡ„ж•Ҹж„ҹжҖ§иҫғе·®пјҢдҪңиҖ…еӣўйҳҹи®ҫи®ЎдәҶдёҖз§ҚвҖңйқһзј–з ҒеўһеҖјвҖқ(NCVA)зЁӢеәҸгҖӮиҜҘзЁӢеәҸиҜўй—®дәҶзј–з ҒзӘҒеҸҳжҳҜеҗҰеўһејәжҪңеңЁйқһзј–з Ғй©ұеҠЁеҹәеӣ зҡ„еҸ‘зҺ°зҺҮпјҢиҖҢйқһеҸӘжңүйқһзј–з ҒзӘҒеҸҳж—¶жүҚиў«жЈҖжөӢеҲ°гҖӮдәҺжҳҜеҸҲиҜҶеҲ«дәҶеҸҰеӨ–31дёӘеҹәеӣ пјҢдёҺ62дёӘеҚ•еҹәеӣ йқһзј–з ҒзӘҒеҸҳеҗҲ并еҗҺеҫ—еҲ°93дёӘеёҰжңүйқһзј–з ҒзӘҒеҸҳзҡ„йҖҡи·Ҝзүөиҝһй©ұеҠЁеҹәеӣ (PID-N)гҖӮеҢ…жӢ¬дәҶ19дёӘе…ҲеүҚж №жҚ®COSMICзҷҢз—Үеҹәеӣ жҷ®жҹҘ(CGC)ж•°жҚ®еә“зЎ®е®ҡзҡ„зҷҢз—Үеҹәеӣ пјҢжҳҫи‘—й«ҳдәҺйў„жңҹзҡ„еҹәеӣ гҖӮеңЁжҺ’йҷӨPCAWGеҲҶжһҗдёӯе…·жңүдёӘдҪ“жҳҫи‘—йқһзј–з Ғе…ғ件зҡ„8дёӘеҹәеӣ пјҢ19дёӘеҹәеӣ еҗҢж—¶дёәPID-Nеҹәеӣ е’ҢCGCеҹәеӣ пјҢжҳҫи‘—еҜҢйӣҶдәҺйў„жңҹзҡ„еҹәеӣ гҖӮ
жҺЁиҚҗйҳ…иҜ»
- еұұдёң|жҺўзҙўйқ’е№ҙеӯҰз”ҹеҠ©еҠӣд№Ўжқ‘жҢҜе…ҙж–°жЁЎејҸпјҢ2020е№ҙвҖңжё…еҚҺеӯҰеӯҗеұұдёңиЎҢвҖқеңҶ满收е®ҳ
- |гҖҠжҲ‘зҡ„еҘіеҸӢжҳҜжңәеҷЁдәәгҖӢйҰ–жӣқиҠұзө®пјҢиҫӣиҠ·и•ҫеҢ…иҙқе°”жҗһжҖӘ
- гҖҗең°иҜ„зәҝгҖ‘е®үе…ЁејҖеӯҰпјҢзІҫз»ҶеҢ–йҳІжҺ§
- гҖҗең°иҜ„зәҝгҖ‘дә¬еҪ©еҘҪиҜ„пјҡж”№йқ©дёҚеҒңйЎҝејҖж”ҫдёҚжӯўжӯҘжҳҜжңҖеҘҪзҡ„зәӘеҝө
- гҖҗең°иҜ„зәҝгҖ‘е®үе…ЁејҖеӯҰпјҢзІҫз»ҶеҢ–йҳІжҺ§|гҖҗең°иҜ„зәҝгҖ‘е®үе…ЁејҖеӯҰпјҢзІҫз»ҶеҢ–йҳІжҺ§
- еӨ–дәӨйғЁеӣһеә”е®үеҖҚжҷӢдёүе®ЈеёғиҫһиҒҢпјҡзҘқж„ҝд»–ж—©ж—Ҙеә·еӨҚ
- ж ҮеҮҶең°еӣҫ|2020е№ҙж ҮеҮҶең°еӣҫеҸ‘еёғпјҢ дёҖзӮ№йғҪдёҚиғҪй”ҷпјҒ
- 2020|йқ’еІӣ银иЎҢе…¬еёғ2020е№ҙдёӯжңҹдёҡз»©пјҡ иө„дә§жҖ»йўқи¶…4405дәҝе…ғ жҢҒз»ӯзЁіеҒҘеўһй•ҝ
- 2020|жү©ж•Је‘ЁзҹҘпјҒиҮӘ然иө„жәҗйғЁпјҡ2020е№ҙж ҮеҮҶең°еӣҫеҸ‘еёғ
- еӨ–дәӨйғЁ|еӨ–дәӨйғЁеӣһеә”е®үеҖҚжҷӢдёүе®ЈеёғиҫһиҒҢпјҡзҘқж„ҝд»–ж—©ж—Ҙеә·еӨҚ



![[з”өи§Ҷеү§]收и§ҶзҺҮй«ҳеҲ°вҖңеҗ“дәәвҖқзҡ„4йғЁз”өи§Ҷеү§пјҢдҪ иӢҘдёҖйғЁжІЎзңӢпјҢеӨӘеҸҜжғңдәҶ](http://img88.010lm.com/img.php?https://image.uc.cn/s/wemedia/s/2020/31d32d4273de006cc8a3ab0e94850c53.jpg)














