文章|2020年10分+纯生信文章带你领略Nature子刊之驱动突变文章套路( 三 )
虽然这些基因表达相关性为一类PID-N基因提供支持,但突变的变异等位基因频率和基因的拷贝数是基因表达的附加协变量。这些协变量在作者发现的相关性中没有发挥作用,拷贝数的变化不影响上述五个PID- N基因的表达相关性。
此外,出现相关基因表达变化的PID-N基因数量少,可以解释为PID-N基因突变的样本数量少,表达数据在不同肿瘤类型间的可用性不均匀,以及启动子区域的序列覆盖率降低等。这些问题进一步减少了非编码突变和RNA表达的样本数量,限制了cis基因表达相关性分析的能力。
3.编码和非编码突变的模块化
在确定了编码突变、非编码突变或两种突变组合改变的特定蛋白质-蛋白质互作亚网络和生物通路后。作者又发现PID-C基因间的交互作用显著增加,以及PID-C和PID-N基因间的互作显著增加。
证明了物理层面的蛋白-蛋白互作网络中编码和非编码突变之间的相互作用。涉及PI-C和PI-N基因的互作子网络组织为五个生物学过程:核心驱动、染色质组织、细胞增殖、发育和RNA剪接(图4a)。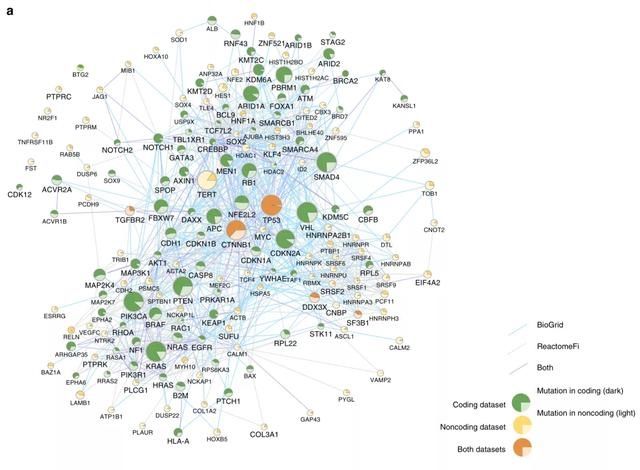
文章图片
▲ Fig.4a
由于PID-C和PID-N基因之间的分子相互作用被用作通路和网络方法的信号,因此作者预计PID-C和PID-N基因之间的分子相互作用频率较高,这些相互作用的组织说明了单个子网络中编码和非编码突变的相对贡献。接下来作者使用g:Profiler web server进一步表征了PID-C和PID-N中富集的分子通路。并将模块和PID基因分成四个生物过程:染色质组织、细胞增殖、发育和RNA剪接(图4b).、
文章图片
▲ Fig.4b
同样,模式规范过程也受到编码和非编码突变的影响,包括PI-N基因ASCL1、SUFU和RELN以及PI-C基因ATM和SMAD4。在这些情况下,非编码突变补充了破坏这些通路的编码突变,覆盖了更多的患者。并且作者惊喜的发现RNA剪接途径主要受到非编码突变的影响。根据PCAWG驱动程序的单一元素测试和功能解释工作组分析,这些PI-N基因均未发生显著突变。由于进一步的分析中没有发现剪接相关的PI-N基因非编码突变和表达改变之间存在显著的顺式关联,因此作者继续探索这些基因非编码突变和其他基因表达之间的潜在反式效应。最终确定了三个集群的RNA剪接基因突变(C1, C2, C3;图5a, b)使用跨这些途径的差异表达模式的分级聚类。
除了上述模块,我们还发现转录因子在PI-C和PI-N基因中都有很好的表达。共有9个PI-C基因是转录因子(ARHGAP35、ARID2、FOXA1、GATA3、NFE2L2、SMAD4、SOX9、TCF7L2、TP53);19个PI-N基因为转录因子(ASCL1、BHLHE40、ESRRG、HES1、HNF1A、HNF1B、HOXA10、HOXB5、KLF4、MEF2C、MYC、NFE2、NR2F1、SOX2、SOX4、TCF4、TP53、ZNF521、ZNF595;FDR= 4.1×10?20)。
这一观察结果表明,非编码突变可能影响转录调控网络。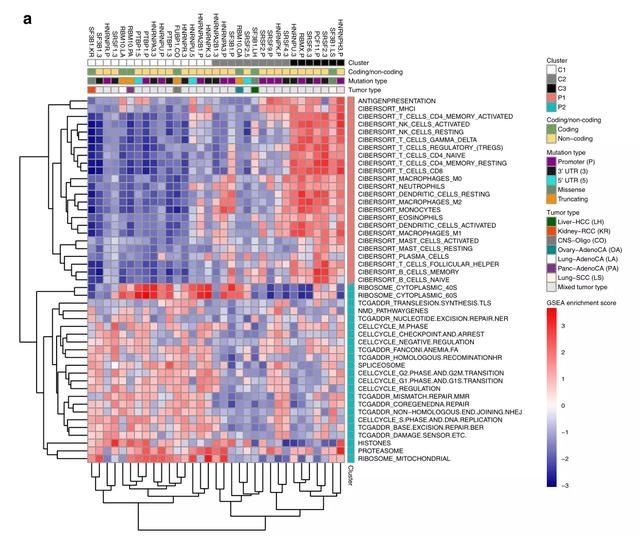
文章图片
▲ Fig.5a
文章图片
▲ Fig.5b
全文思路总结
范文提出了一种综合途径和网络分析,将可能发生非编码驱动突变的基因列表扩展为很少突变的元素的“长尾”,而单一元素分析并不显著。通过对非编码突变数据的单一元素测试,90个PI-N基因在统计学上不显著(FDR > 0.1),而这些基因是未来实验表征的关键候选基因。并发现其中TP53、TLE4、TCF4启动子突变与这些基因表达降低有关。随后的通路分析中,作者又发现了多个基因的非编码突变,这些突变的样本表现出的基因表达特征与编码突变剪接因子样本的基因表达变化一致。表明罕见的非编码突变可能导致共同的和互补的生物学过程相似的干扰。
同时作者指出,进一步的实验验证这些预测是必要的,以确定PID基因列表的真实性。由于单个癌症类型的作用有限,通路和互作网络分析更加侧重于癌症和组织类型之间的关联。
每种细胞类型都有不同的表观遗传连接和调控机制,非编码突变可能针对细胞类型相关的漏洞。将组织特异性、癌症特异性或患者特异性基因-基因调控信息结合起来的方法,可能会揭示出目前的方法还没有探索过的一类新的驱动因素。这篇文章提出了一种综合途径和网络分析,可以很好的解释肿瘤基因组的编码和非编码景观,从而发现相互关联的基因系统中的驱动机制。通过扩展突变分析,从单个基因组元素到多个基因的通路和网络,从中确定了已知癌症通路中的新成分,这些成分因被编码和非编码突变反复改变,从而可能在癌症中起到重要作用。
并且作者团队还确定了新的路径和子网络。对干扰这些通路和网络的编码和非编码突变的研究能够将患者分层策略更精确,以通路为重点的生物标志物和治疗方法成为可能。
套路总结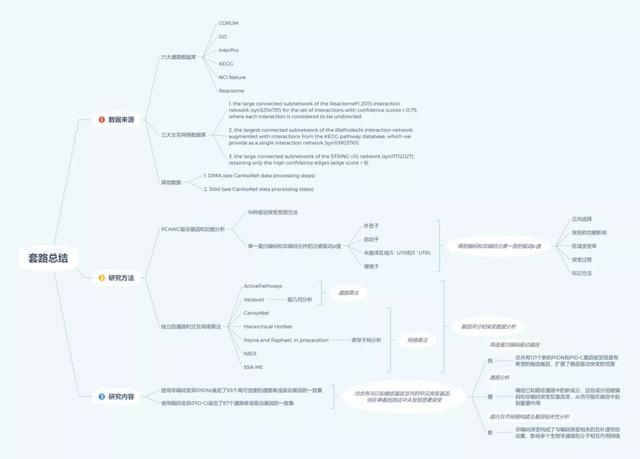
文章图片
总之,生信文章如何能发高分?必须具有临床意义!
能够为基础及临床试验提供可靠的数据支持,预测可能存在的具有临床意义的结果是生信分析的意义所在和终极目标。本篇范文就是在先前研究的庞大且精准的数据库的基础上进行数据挖掘,从通路和蛋白互作网络的角度分析可能存在的肿瘤驱动突变发病的临床意义和机制。鉴定出的基因变异可用于将患者分类,便于接受已批准的或正在临床试验的治疗,体现了肿瘤全基因组图谱对癌症精准医学的重要性。
推荐阅读
- 山东|探索青年学生助力乡村振兴新模式,2020年“清华学子山东行”圆满收官
- |《我的女友是机器人》首曝花絮,辛芷蕾包贝尔搞怪
- 【地评线】安全开学,精细化防控
- 【地评线】京彩好评:改革不停顿开放不止步是最好的纪念
- 【地评线】安全开学,精细化防控|【地评线】安全开学,精细化防控
- 外交部回应安倍晋三宣布辞职:祝愿他早日康复
- 标准地图|2020年标准地图发布, 一点都不能错!
- 2020|青岛银行公布2020年中期业绩: 资产总额超4405亿元 持续稳健增长
- 2020|扩散周知!自然资源部:2020年标准地图发布
- 外交部|外交部回应安倍晋三宣布辞职:祝愿他早日康复









![[俄罗斯观察者]油价下跌将导致危机,萨卡什维利预测:乌克兰政府不会治理国家](https://imgcdn.toutiaoyule.com/20200322/20200322164237960412a_t.jpeg)









